Libreta de apuntes
Enlaces relacionados
- Ácidos orgánicos
- Aditivos alimentarios
- Alcaloides
- Alelopatía
- Almendra
- Aminoácidos
- Aminoácidos esenciales
- Antioxidantes
- Cafeína
- Capsaicina
- Carotenoides
- Catequinas
- Cumarinas
- Disacaridos
- Diterpenos
- Ester
- Esteroides
- FENILETILAMINA
- Fenol
- Fenoles
- Fitoalexinas
- Fitoesteroles
- Flavonoides
- Hidratos de carbono
- Glucosa
- GUARANINA
- Inulinas
- Irioides y sesquiterpenos
- Isoflavonas
- Lípidos
- Lipoproteínas
- MATEÍNA
- Monosacáridos
- Oligoelementos
- Oligosacáridos
- Polifenoles
- Polisacáridos
- Prostaglandinas
- Proteínas
- Quinina
- Quinonas
- Radicales libres
- RESVERATROL
- Saponinas
- Taninos
- TEÍNA
- Teobromina
- Teofilina
- Terpenos
- Triglicéridos
- Triperpenos y esteroides
- Vitaminas
ÍNDICE
La página de Bedri
żQué son los alcaloides ?
Los alcaloides son compuestos orgánicos nitrogenados, derivados a partir de un aminoácido, de carácter alcalino producidos casi exclusivamente por vegetales aunque también los hay producidos por animales y hongos, y otros sintetizados químicamente.
El nombre procede de álcali, carbonatos de alcalinos, y -oide, parecido a, y se refiere a aquellos metabolitos secundarios de las plantas sintetizados, generalmente, a partir de aminoácidos. Los alcaloides verdaderos derivan de un aminoácido, son por lo tanto nitrogenados. Son básicos (excepto colchicina) y poseen acción fisiológica intensa en los animales aun a bajas dosis con efectos psicoactivos, por lo que son muy usados en medicina para tratar problemas de la mente y calmar el dolor. Ejemplos conocidos son la cocaína, la morfina, la atropina, la colchicina, la quinina, cafeína y la estricnina.
Generalidades
Existen aproximadamente unos 5000 alcaloides que no son exclusivos de los vegetales ya que se han encontrado también dentro del reino animal. Algunos de ellos los podemos encontrar en la piel de ciertos animales, como la bufonina, que segregan los sapos o la batracotoxina de las ranas del genero Phyllobates , uno de los más potentes del mundo, especialmente el de la especie Phyllobates terribilis capaz de matar a 10 hombres con 1 miligramo de la misma. Curiosamente este alcaloide también aparece en las plumas de los pájaros del género Pitohui de Nueva Guinea y que produce una paralización en el miembro que lo toca. Otros alcaloides son elaborados por pequeńos animales como ciempiés, hormigas, mariquitas, etc. Otro alcaloide de origen animal es como la samandarina de las glándulas de la piel de Salamandra maculosa.
La mayoría de los alcaloides, sin embargo, pertenecen al reino vegetal, de tal manera que un 10 % del total de las especies vegetales contienen alguno de estos compuestos. Aparecen a veces en toda la planta, como, por ejemplo, el tejo ( Taxus bacata ) un árbol cuya única parte comestible es el arilo extremadamente apreciado por los pájaros. El resto es venenoso.
Generalmente en las plantas no se encuentran como bases libres sino en forma de sales unidos a ácidos orgánicos banales como el ácido cítrico, málico, succínico, etc. En algunas ocasiones se unen a ácidos orgánicos específicos como al ácido mecónico en el opio o al ácido trópico en las Solanáceas tropánicas. También se encuentran a veces unidos a taninos o a azúcares, otras veces están como amidas o como ésteres. Normalmente se trata de bases débiles, pero algunos son bases fuertes o también compuestos neutros o anfóteros, es decir que pueden actuar a la vez como bases y como ácidos.
Estructura química
Sus estructuras químicas son variadas, los alcaloides poseen una gran diversidad estructural con mas de 12.000 estructuras. Se considera que un alcaloide es, por definición, un compuesto químico que posee un nitrógeno heterocíclico procedente del metabolismo de aminoácidos; de proceder de otra vía, se define como pseudoalcaloide.
Propiedades físico-químicas
La presencia de oxígeno en la estructura determina que la sustancia sea un sólido blanco, de sabor amargo y cristalizables. La ausencia de oxígeno en la estructura del alcaloide hace que éste sea aceitoso, volátil u odorante.
La mayoría de los alcaloides son insolubles o muy poco solubles en agua, pero se disuelven bién en alcohol, éter, cloroformo u otros solventes orgánicos.
Se combinan con ácidos para dar sales, comportándose entonces como bases. Las sales son bastante solubles en agua e insolubles en solventes orgánicos.
En la diferencia de solubilidades de la base alcaloidea y de sus sales en agua y en solventes orgánicos se basa el método general de extracción.
Todos los alcaloides son activos a la luz polarizada. Presentan una fluorescencia característica bajo al luz UV o IR, dando lugar a espectros característicos.
Clasificación
Su clasificación es compleja pudiéndose acometer desde distintos puntos de vista. En el momento actual parece ser la clasificación biogenética la de elección, es decir, según su origen o formación en el vegetal. Esta clasificación está bastante relacionada, en la mayoría de los casos, con la clasificación química que venía siendo la utilizada en tiempos anteriores.
Así, puesto que una gran parte de los alcaloides derivan de unos pocos aminoácidos, bien de cadena abierta o aromáticos, la clasificación puede realizarse de la siguiente forma:
- Alcaloides derivados de ornitina y lisina: tropánicos, pirrolizidínicos, piperidínicos y quinolizidínicos.
- Alcaloides derivados del ácido nicotínico.
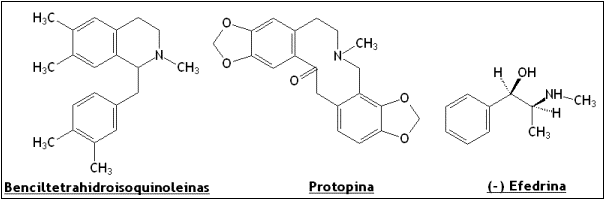
- Alcaloides derivados de fenilalanina y tirosina: feniletilamínicos e isoquinoleínicos.
- Alcaloides derivados del triptófano: indólicos y quinoleínicos.
- Alcaloides derivados de la histidina: imidazólicos
- Alcaloides derivados del ácido antranílico.
- Alcaloides derivados del metabolismo terpénico: diterpénicos y esteroídicos.
- Otros alcaloides: bases xánticas.
Efectos biológicos
Generalmente actúan sobre el sistema nervioso central, si bien algunos afectan al sistema nervioso parasimpático y otras al sistema nervioso simpático, por ejemplo, la cocaína actúa impidiendo la recaptación de dopamina de la terminal sináptica, lo que produce un mayor efecto de los receptores dopaminérgicos.
La actividad biológica de los alcaloides es muy diversa, la más estudiada es la acción euforizante que presentan algunos como la cocaína, si bien también existen alcaloides con efectos depresores del sistema nervioso central como la morfina.
Función en los vegetales
Se ha discutido mucho sobre la función que los alcaloides desempeńan en el mundo vegetal sin que se haya llegado a dar ninguna razón concluyente. Entre las muchas interpretaciones tendríamos las siguientes:
Valor defensivo: Se ha considerado estos compuestos como una manera que tienen los vegetales de protegerse frente a la agresión de los animales , lo cual parece ser solamente cierto en parte porque en muchos casos estos productos tienen poco efecto en los mismos. Es curioso, por ejemplo, el caso del escarabajo del Colorado (Leptinotarsa decemlineata) cuyas larvas pueden alimentarse de hojas de solanáceas como el tomate, la patata o incluso belladona sin que sus peligrosos alcaloides lleguen a afectarle.
Valor hormonal: Su función sería equivalente a la que realizan las hormonas e equiparables a la hormona animal adrenalina. Lo cierto es que suele coincidir los niveles más altos de los mismos con los momentos de metabolismo más intenso.
Valor alelopático: Según esta interpretación, las plantas utilizarían los alcaloides para influir positiva o negativamente sobre otras especies próximas, bien para comunicarse con especies similares o inhibir el crecimiento de otras que podrían resultarles competitivas, como la cocaína, la cafeína o la estricnina que impide el crecimiento de otras especies junto a ellas. (Ver más de la alelopatía)
Efectos en los humanos
Sistema nervioso: Algunos ejercen una función estimulante del sistema nerviosos central (SNC) como la cafeína (café y especialmente en el té ), la teobromina (cacao) o la estricnina (nuez vómica ) que, en dosis muy pequeńas también resulta convulsivo. Otros, como la escopolamina del beleńo (Hyoscyamus niger) ejercen una función tranquilizante, de ahí que se utilizan en medicina como sedantes. La morfina, un derivado del opio que se extrae del látex de la cápsula de la adormidera (Papaver somniferum) constituye el principal somnífero. Hay también algunos, como la aconitina (acónito) que, aunque inicialmente sean estimulantes, posteriormente son paralizantes.
Músculos: Pueden afectar a toda la musculatura, produciendo espasmos violentos y muy dolorosos, como la estricnina, que causa grandes convulsiones que conducen a la muerte por asfixia o agotamiento. También pueden actuar sobre ciertos músculos concretos, provocando su dilatación, tal como ocurre con la escopolamina (beleńo) responsable de la midriasis o dilatación de la pupila. El efecto contrario lo provocan otros como la eserina que contiene el haba calabar (Physostigma venenosum) que se utiliza en oftalmología para contraer las pupilas de los ojos, o la digitalina de las digitalis o dedaleras (Digitalis sp) que actúa sobre el músculo cardíaco.
Sistema digestivo: Algunos son muy tóxicos para el aparato digestivo, produciendo irritaciones violentas de todas las mucosas gástricas con manifestaciones tan típicas como diarreas, vómitos, etc. Entre estos uno de los mas venenosos son las semillas del ricino (Ricinus communis) que contienen el alcaloide ricinina, cuyas propiedades se han utilizado como purgante, aunque resulta extremadamente peligroso, dado que un par de semillas bien masticadas pueden resultar mortales para un nińo. Igualmente agresivo para el estómago constituye la colquicina del cólquico (Colchicum autumnale). Hay que mencionar aquellos que atacan el hígado causando lesiones hepáticas como cirrosis, hepatitis, cáncer, etc., como la cinoglisina del heliotropo (Heliotropium europaeum).
Sistema circulatorio: su efecto se realiza sobre los vasos circulatorios como la reserpina de la Rauwolfia vomitoria que baja la presión sanguínea, por lo que se utiliza para tratar la hipertensión. Alcaloides que ejercen un efecto contrario serían, por ejemplo, la esparteína de la retama negra (Cytisis scoparius) cuyas propiedades hipertensivas se han aprovechar para incrementar el metabolismo y propiciar la eliminación de líquidos en personas afectadas por obesidad.
Aparato respiratorio: Dentro de este apartado tenemos alcaloides que tienen la propiedad de dilatar los bronquios posibilitando un aumento de la respiración Así, la escoparina contenida en las flores de la retama negra (Cytisis scoparius) ha sido utilizada para combatir enfermedades respiratorias. Igualmente la efedrina, un alcaloide con propiedades similares a la adrenalina producido por especies distintas de del genero Ephedra, se ha utilizado como descongestionante en el tratamiento de afecciones bronquiales y asma, además de poseer propiedades estimulantes. La FDA (Dirección de alimentos y drogas en USA) ha prohibido su uso recientemente. Muchos alcaloides que actúan sobre el aparato respiratorio, cuando superan las dosis permitidas, producen parada respiratoria.
Efectos psicotrópicos
Otros alcaloides formarían parte del grupo de los llamados psicotrópicos, que son aquellos que afectan a la mente , alterando la percepción. Entre ellos tendríamos que mencionar:
Alucinógenos: que producen alucinaciones o alteraciones en el pensamiento, sentimiento o percepción en forma de ilusiones distorsionadas de la realidad o de percepción de realidades inexistentes. Dentro de este apartado tendríamos Tóxicos comola mezcalina que forman parte del peyote (Lophophora williamsii), la cannabina del cannabis (Cannabis sativa)o la harmalina de la ruda siria (Peganum harmala), la ergotoxina del cornezuelo del centeno (Claviceps purpurea), la Muscarina del hongo Amanita (Amanina muscarina).
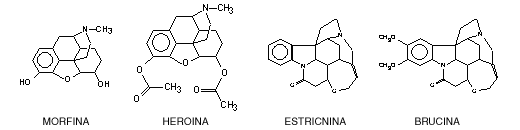
Narcóticos: alcaloides que provocan narcosis, es decir que inducen a un estado de somnolencia. Se utilizan medicinalmente como analgésicos, aunque crean dependencia por lo que se su uso legal viene regulado médicamente. Dentro de esta categoría tendríamos fundamentalmente los opiáceos, como el opio que se extrae del látex de la adormidera (Papaver somniferum). A partir de él se produce la morfina, el principal analgésico. La codeína y la heroína se obtienen a partir de esta última.
Estimulantes: producen un estado de euforia y bienestar. Entre estos tendríamos alcaloides tan conocidos como la cocaína que se extrae de las hojas de la coca (Erythroxylon coca), muy utilizado por las poblaciones andinas como euforizante, para combatir el mal de altura y permitir un rendimiento superior en el trabajo, a parte de muchas otras propiedades medicinales que le atribuyen sus usuarios. Otro alcaloide dentro de este grupo es la nicotina, que se obtiene del tabaco (Nicotiana tabacum)y de la mayoría de los miembros de la familia de las solanáceas, un estimulante que también crea dependencia , además de un veneno mortal en dosis muy bajas. Finalmente, mencionaremos la cafeína, alcaloide presente en plantas como el café (Coffea arabica L.), el té (Camellia sinensis (L.) KUNTZE ), el mate (Ilex paraguensis), el cacao (Theobroma cacao L.); el naranjo, (Citrus sinensis (L.) OSBECK), el limonero (Citrus limon (L.) BURMAN f.) Excita el sistema nervioso, aumenta el ritmo cardíaco y favorece la eliminación de la orina. Un uso prolongado y abundante produce sobreexcitación, impide el sueńo e irrita la mucosa gástrica. No resulta muy adictivo.
Historia
El aislamiento de los primeros alcaloides en el siglo XIX coincidió más o menos con la introducción del proceso de percolación para la extracción de las drogas. El farmacéutico francés Charles Derosne probablemente aisló en 1803 el alcaloide denominado después narcotina, y el farmacéutico Friedrich Sertüner investigó sobre el opio y aisló la morfina. A ello siguió rápidamente el aislamiento de otros alcaloides como la estricnina, cafeína, entre otros.
La coniína es el alcaloide más antiguo en cuanto al establecimiento de su estructura y de su síntesis, pero otros, como la colchicina, necesitaron más de un siglo para que sus estructuras fuesen definidas.
Extracción
Los métodos de extracción son muy variados, pero últimamente está adquiriendo fuerza la purificación por medio de fluidos supercríticos, concretamente con dióxido de carbono. Para obtener los alcaloides de los vegetales, se extraen de las partes de la planta que los contienen, con agua si están en forma de sales (solubles) o con ácido clorhídrico diluido si están en forma insoluble.
Detección e identificación
Los alcaloides, junto a otras drogas básicas de interés toxicológico, tienen un comportamiento análogo frente a un grupo de reactivos de precipitación que permiten sospechar su presencia. en una pericia toxicológica se hace uso de estas reacciones como primer paso de identificación, y a que una reacción positiva excluye la presencia de estos tóxicos, aunque una reacción positiva no asegura su presencia.
La reacción con el Reactivo de Mayer (tetraiodo mercuriato de potasio) da lugar a la formación de un precipitado amarillento amorfo o cristalino.
El Reactivo de Draggendorf (yodo bismutato de potasio) forma precipitados de dolor rojo anaranjado y en general amorfos.
El Reactivo de Bouchardat (triioduro) genera precipitados de color rojo pardo.
El procedimiento para estos reactivos generales comienza con la evaporación de 2 a 3 gotas del extracto etanólico en vidrio de reloj. Se agregan luego 2 a 3 gotas de ácido clorhídrico 5% hasta solubilizar los residuos. A esta solución se agrega una gota del reactivo correspondiente.
Genalcaloides
Los genalcaloides, u óxidos aminados de alcaloide, son derivados por oxidación de los alcaloides que contienen el grupo R=(NO)-R, donde el nitrógeno tiene valencia V, en contraposición a los alcaloides normales, donde es trivalente (R=N-R). Su acción es la misma que la del alcaloide del cual provienen, pero es más pausada. Se nombran ańadiendo el prefijo gen- al nombre del alcaloide. Algunos genoalcaloides se encuentran en la naturaleza, como la geneserina (derivado del alcaloide eserina (fisostigmina)) presente en la Physostigma venenosum o haba de Calabar.
Químicamente pueden ser considerados como -heterocíclicos nitrogenados- derivados de aminoácidos y de los triterpenos. se encuentran formando sales con el ácido acético, oxálico, láctico, málico, tartárico y cítrico. sus actividades biológicas son importantes por su mimetismo hormonal y su intervención en las reacciones principales del metabolismo celular. A pesar de ser sustancias poco similares entre ellas desde el punto de vista estructural, poseen propiedades fisiológicas análogas. Estos compuestos están ampliamente distribuidos en el reino vegetal (25% de las plantas contienen alcaloides) y en algunas especies su concentración puede alcanzar el 10% (flores). Muchos alcaloides son la causa de intoxicaciones en humanos y animales. La forma más común es la intoxicación por infusiones con hierbas con fines medicinales, siendo esta una causa importante de muerte sobre todo en nińos. Su presencia en vegetales hace posible su incorporación accidental en alimentos, creando una vía fácil de intoxicación. Para entender el origen estructural de estos compuestos se les suele clasificar así:
Alcaloides de núcleo pirídico: a
este grupo pertenecen la nicotina, la pilocarpina y la esparteína.
La nicotina se encuentra en el jugo del tabaco acompańada de otros
alcaloides. Es un liquido incoloro de olor semejante al tabaco y sabor
ardiente y picante. Es muy tóxica en dosis altas.
Alcaloides de núcleo isoquinoleico: se encuentran en las plantas
papaveráceas y ranunculáceas. El más importante es la papaverina, que
tiene propiedades hipnóticas (aunque no tan acentuadas como las de la
morfina).
Alcaloides de núcleo fenantrénico: el más importante es la
morfina. Se encuentra en el opio en forma de sal. Se emplea en medicina
en forma de clorhidrato y sulfato, como sedantes y calmantes.
Alcaloides de núcleo tropánico: pertenecen a este grupo la
atropina y la cocaína.
La atropina se encuentra en el jugo de varias plantas como la belladona
y el estramonio.
La cocaína se extrae de las hojas de coca, es de sabor amargo,
insensibiliza la lengua, y se usa en medicina en forma de clorhidrato.
Alcaloides de núcleo indólico: los más importantes son la
estricnina y la brucina.
La estricnina es uno de los alcaloides más enérgicos, se extrae de
diversas plantas del género Strychnos, entre ellas el haba de San
Ignacio y de la nuez vómica. Es de sabor amargo muy intenso y muy
tóxica. su ingestión produce convulsiones tetánicas.
Alcaloides de núcleo no definido: son todos aquellos alcaloides
cuya constitución no ha sido aún establecida con claridad. Entre ellos
se encuentra la aconitina (veneno muy violento, utilizado en terapéutica
para combatir ciertas dolencias) y la ergotinina (uno de los principios
activos del cornezuelo de
centeno,
que ejerce una acción específica sobre el útero.
Los alcaloides pirrolidínicos están asociados a estructuras de pirrolizidinas son metabolitos secundarios de una gran variedad de plantas, que incluye especies que se encuentran en todo el mundo. estas plantas son la causa de numerosos casos de envenenamiento de ganado, y ha causado grandes pérdidas económicas. También son causa de muerte en humanos, especialmente en países poco desarrollados, como consecuencia de la contaminación de cereales y semillas por lo que son de gran importancia en el campo de los alimentos. Se cree que la ingestión de hierbas y vegetales que contienen estos alcaloides, son causa de dolencias. La estructura de estos alcaloides esta basada en dos anillos de 5 átomos unidos que comparten un átomo de nitrógeno. en la naturaleza por lo general los anillos tienen como sustituyentes grupos hidroximetileno en la posición c-1 y grupos hidroxilos en c-7; esta estructura se conoce como necina. ejemplos típicos de esta base son la heliotridina y la retronecina.
Las pirrolizidinas se encuentran principalmente en las familias Compositae, Boraginaceae, Leguminosae y Apocynaceae. Los géneros productores de estos alcaloides están distribuidos en diferentes regiones y climas y podrían representar hasta el 3% de las plantas con flores. Algunas contienen una sola clase de pirrolizidina pero la mayoría contienen entre cinco y ocho clases. El contenido varía con cada especie, pero puede llegar a ser un porcentaje importante del peso seco. La mayor concentración se encuentra en raíces y es mayor en hojas jóvenes, inflorescencias y capullos que en hojas más viejas. En algunas especies se encontraron altas concentraciones en semillas, lo que implica un riesgo en los casos en que estas semillas sean utilizadas para la alimentación humana. Existen N-óxidos de estos alcaloides, que son más solubles en agua y son transportados más fácilmente dentro de la planta.
Usos y aplicaciones
Muchos tienen un sabor amargo. Cumplen diversas funciones en las plantas, como defensas naturales contra animales y hongos, y suelen producir efectos fisiológicos en los animales. Es decir, son drogas, y como tales, según la dosis, y la duración del tratamiento, sus usos (en Medicina) pueden ser desde analgésicos, anestésicos o curativos de ciertas enfermedades, hasta producir la muerte (empleados como pesticidas, insecticidas o armas criminales), y/o producir adicciones leves o graves.
Dada la actividad/toxicidad tan marcada en muchos de estos compuestos, en bastantes ocasiones no se emplean las plantas que contienen alcaloides sino los alcaloides aislados de las mismas, bien controlados y dosificados.
Lista de algunos de los alcaloides más importantes
| Aconitina | |
| Obtención | Acónito |
| Propiedades físico-químicas | Soluble en cloroformo o benceno |
| Propiedades biológicas | Altamente venenoso, neurotoxina |
| Usos medicinales | Para crear modelos de arritmia cardíaca |
| Fórmula química | C34H47NO11 |
| Adrenalina | |
| Obtención | Sintetizado a partir de la efedrina. Tiene muchos derivados. |
| Propiedades físico-químicas | Imita la acción de la hormona adrenalina, amina simpaticomimética de acción central. |
| Propiedades biológicas | Fuerte estimulante del sistema nervioso central, mejora el estado de vigilia, alerta y atención. |
| Usos medicinales | Trastorno por déficit de atención con hiperactividad, narcolepsia y depresión refractaria. |
| Uso recreativo-ilegal | Se emplean derivados para pasar la noche sin dormir en discotecas, que pueden producir crisis de paranoia y ansiedad, y psicosis anfetamínica. |
|
Fórmula química |
C9H13N. |
| Atropina | |
| Obtención | De plantas solanáceas como la belladona, un arbusto venenoso. Aislada por primera vez en 1831 por Mein. |
| Etimología: | De Átropos, la mayor de las tres moiras en la mitología griega, la que cortaba el hilo de la vida de cada mortal. |
| Propiedades biológicas | Droga anticolinérgica. |
| Usos medicinales | Considerada por la OMS una medicina esencial. Para dilatar las pupilas, en trastornos cardíacos (activar el ritmo cardíaco), como antídoto por envenenamiento con insecticidas organofosforados y gases nerviosos (uso militar), etc. |
| Fórmula química | C17H23NO3 |
| Cafeína | |
| Obtención | Del fruto del cafeto. Descubierta en 1819 por Ruge. |
| Nombres alternativos | Cuando se extrae del guaraná se llama guaranina, del mate se llama mateína y del té, teína, pero son el mismo alcaloide. |
| Familia | Metilxantina |
| Propiedades biológicas | Estimulante adictivo del sistema nervioso autónomo, estimulando el estado de vigilia, la resistencia al cansancio y vasoconstricción cardíaca. La sobredosis produce insomnio, nerviosismo, etc. Pesticida natural contra ciertos insectos comedores de plantas. |
| Usos medicinales |
Contra la cefalea, asma bronquial, cólicos de la vesícula biliar. |
| Fórmula química | C8H10N4O2 |
| Ver más de la cafeína | |
| Capsaicina | |
| Obtención |
De los pimientos picantes. |
| Propiedades biológicas |
Es un irritante, produciendo una sensación de quemazón. |
| Usos | En alimentación, como condimento. En medicina, contra el dolor. En defensa personal, en sprays defensivos contra delincuentes. |
| Fórmula química | C18H27NO3 |
| Ver más de la capsaicina | |
| Cocaína | |
| Obtención | De la hoja de la coca. |
| Propiedades biológicas | Estimulante adictivo del sistema nervioso central, concretamente del sistema dopaminérgico. |
| Usos | Puede ser empleada en cirugía como anestésico. Famosa droga ilegal. |
| Fórmula química | C17H21NO4 |
| Codeína (metilmorfina) | |
| Obtención | Del opio |
| Usos medicinales |
Es un calmante similar a la morfina, pero menos potente (y menos adictivo). También se usa contra la tos. |
| Fórmula química | C18H21NO3. |
| Colchicina | |
| Obtención |
Extraída originalmente de plantas del género colchicum. |
| Propiedades biológicas | Venenosa |
| Usos medicinales |
Se usa actualmente en el tratamiento de la gota y se investigan sus posibles propiedades anticancerígenas. |
| Fórmula química | C22H25NO6. |
| Conicina | |
| Obtención | Se encuentra en la cicuta. Fue el primer alcaloide sintetizado, en 1886 por Albert Ladenburg. |
| Usos medicinales |
Neurotoxina. Sócrates fue ejecutado haciéndole tomar cicuta. |
| Fórmula química | C8H17N |
| Efedrina | |
|
Obtención |
Extraída originalmente de ephedra vulgaris. |
|
Propiedades biológicas |
Estimulante del sistema nervioso simpático. |
|
Usos medicinales |
Como descongestionador nasal, broncodilatador, etc. También se usa mucho en medicina tradicional china. |
|
Fórmula química |
C10H15NO |
| Ergotamina | |
| Obtención | Es el principal alcaloide del cornezuelo, un hongo parásito que afecta sobre todo al centeno. Es un precursor del LSD. |
| Usos medicinales | Se usa como vasoconstrictor para prevenir la migrańa. |
| Fórmula química | C33H35N5O5 |
| Escopolamina | |
| Obtención | Se encuentra en solanáceas (escopolia, beleńo, mandrágora, etc.). |
| Propiedades biológicas | Depresor de las terminaciones nerviosas y el cerebro, y antagonista de las sustancias que estimulan el sistema nervioso parasimpático. Produce somnolencia y pérdida temporal de memoria. |
| Usos medicinales | Se emplea para tratar el mareo y náuseas en viajes, como antiparkinsoniano y para dilatar las pupilas en oftalmología. |
| Fórmula química | C17H21NO4 |
| Estricnina | |
| Obtención | Extraído de la nuez vómica. |
| Propiedades biológicas | Es un potente veneno y estimulante del sistema nervioso central |
| Usos | Se emplea como pesticida, para matar ratas. |
| Fórmula química | C21H22N2O2 |
| Gramina | |
| Obtención | Aunque se encuentra en varias especies de plantas, es más fácil sintetizarlo químicamente. |
| Usos | Se emplea para sintetizar triptófano. |
| Fórmula química | C11H14N2 |
| Heroína (diacetilmorfina) | |
| Obtención | Sintetizada en 1883 por Heinrich Dreser a partir de la morfina. |
| Propiedades biológicas | Al igual que ésta, es analgésica, pero también tiene ciertos efectos estimulantes. Es muy adictiva y es el opiáceo de acción más rápida. Más potente que la morfina pero menos duradero. |
| Usos | Famosa y peligrosa droga ilegal. |
| Fórmula química | C21H23NO5 |
| Higrina | |
| Obtención | Se encuentra en las hojas de coca. Fue aislado por primera vez en 1889 por Carl Liebermann. |
| Fórmula química | C8H15NO |
| Hioscina | |
| Obtención | Se encuentra en solanáceas (escopolia, beleńo, mandrágora, etc.). |
| Propiedades biológicas | Depresor de las terminaciones nerviosas y el cerebro, y antagonista de las sustancias que estimulan el sistema nervioso parasimpático. Produce somnolencia y pérdida temporal de memoria. |
| Usos medicinales | Se emplea para tratar el mareo y náuseas en viajes, como antiparkinsoniano y para dilatar las pupilas en oftalmología. |
| Fórmula química | C17H21NO4 |
| Mescalina (trimetoxifeniletilamina) | |
| Obtención | Aislado del peyote y otras plantas cactáceas. |
| Propiedades biológicas | Es un alucinógeno. |
| Fórmula química | C11H17NO3 |
| Morfina | |
| Obtención | Se extrae del opio. Conocida desde 1688, parece ser que fue aislada en 1803 por De Rosne. |
| Etimología | Su nombre proviene de Morfeo, el dios de la mitología griega del sueńo. |
| Propiedades biológicas | Fuertes propiedades narcóticas y anestésicas. Muy adictiva. |
| Usos medicinales | Es el más utilizado contra el dolor, especialmente el grave. |
| Fórmula química | C17H19NO3 |
| Muscarina | |
| Obtención | Aislada originalmente del hongo amanita muscaria (hongo mosca) en 1869. |
| Propiedades biológicas | Es un fuerte activador del sistema nervioso parasimpático periférico, pudiendo llegar a la muerte (su antídoto es la atropina). |
| Fórmula química | C9H20NO2+ |
| Muscimol | |
| Obtención | Es el principal alcaloide psicoactivo del género de hongos amanita. |
| Propiedades biológicas | Es un alucinógeno |
| Fórmula química | C4H6N2O2 |
| Nicotina | |
| Obtención | Se extrae del tabaco. |
| Etimología | Su nombre procede de Jean Nicot, que introdujo el tabaco en Francia en 1560. |
| Propiedades biológicas | Es un potente veneno que a bajas dosis es estimulante. Causa la adicción al tabaco. |
| Usos | Como insecticida en fumigación en invernaderos. |
| Fórmula química | C10H14N2 |
| Papaverina | |
| Obtención | Se extrae de la amapola del opio. |
| Usos medicinales | En el tratamiento de espasmos viscerales, vasoespasmos (corazón y cerebro), disfunción eréctil, etc. |
| Fórmula química | C20H21NO4 |
| Pilocarpina | |
| Obtención | Se extrae de la hoja de los arbustos pilocarpus, un arbusto tropical americano. |
| Usos medicinales | Se usa en el tratamiento del glaucoma, y como antídoto de la atropina. |
| Fórmula química | C11H16N2O2 |
| Piperina | |
| Obtención | Se extrae de la pimienta negra. |
| Propiedades físico-químicas | Es responsable de la acritud de la pimienta negra. |
| Usos medicinales | En medicina tradicional y como insecticida. |
| Fórmula química | C17H19NO3. |
| Psilocibina | |
| Obtención | Se extrae del género de hongos psilocybe |
| Propiedades biológicas | Es un alucinógeno |
| Fórmula química | C12H17N2O4P |
| Quinina | |
| Obtención | Se extrajo originalmente de la corteza de la quina, árbol originario de Sudamérica, en 1820, por los investigadores franceses Pierre Joseph Pelletier y Joseph Caventou. |
| Etimología | Su nombre procede del idioma quechua |
| Propiedades biológicas | Famosa por ser utilizada contra la malaria. |
| Usos medicinales | Se utiliza para combatir la malaria |
| Fórmula química | C20H24N2O2 |
| Ver más de la quinina | |
| Reserpina | |
| Obtención | Aislada en 1952 de la raíz desecada de rauwolfia serpentina. |
| Usos medicinales | Contra la hipertensión arterial. |
| Fórmula química | C33H40N2O9 |
| Teobromina | |
| Obtención | En el árbol del cacao, (aislado por primera vez en 1878), y por lo tanto, en el chocolate (sobre todo, el chocolate negro). |
| Familia | Metilxantina. |
| Propiedades biológicas | Estimulante del sistema nervioso central (menos que la cafeína) y broncodilatador. Causa posiblemente adicción al chocolate. En perros, gatos, y otros animales es tóxica. |
| Fórmula química | C7H8N4O2 |
| Ver más de la teobromina | |
| Teofilina | |
| Obtención | En el té negro y en el té verde |
| Familia | Metilxantina |
| Propiedades biológicas | Es un estimulante del sistema nervioso central y broncodilatador. |
| Usos medicinales | Como diurético. |
| Fórmula química | C7H8N4O2 |
| Ver más de la teofilina | |
Documentación
http://www.biol.unlp.edu.ar
http://www.botanical-online.com
http://es.wikipedia.org/
http://www.portalfarma.com
http://www.slideshare.net/fabiman/
http://qbitacora.wordpress.com